(2011南京)电解水实验可以确定水的组成。甲、乙、丙三位同学对电解水后液体的酸碱性进行探究。
【提出问题】电解水后的液体一定呈中性吗?
【查阅资料】
图Ⅰ所示装置可用于电解水实验;
硫酸钠可增强水的导电性,硫酸钠溶液呈中性。

【实验与讨论】
三位同学分别向U形管中加入含有酚酞的硫酸钠溶液,接通直流电,观察现象,电解一段时间后,断开电源。
(1)实验中发现管①电极附近的溶液迅速变红,管②电极附近的溶液仍为无色,乙同学用pH试纸测定管②电极附近的溶液,pH小于7。说明管①电极附近的溶液呈 性,管②电极附近的溶液呈 性。(填“酸”、“碱”或“中”)
(2)甲同学将实验后U形管中的溶液按图Ⅱ所示倒入烧杯中,发现红色立刻消失。
乙同学、丙同学将试验后U形管中的溶液按图Ⅲ所示分别倒入烧杯中,发现红色不完全消失。
经讨论与分析,乙、丙同学的试验中溶液的红色不消失,原因可能是酸 。
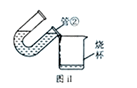
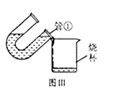
(3)甲、乙、丙同学分别用蒸馏水洗涤U形管、碳棒等,再将洗涤液倒入自己实验的烧杯中,观察现象:
甲同学的溶液仍为无色。
乙同学的溶液中红色仍不消失。
丙同学的溶液中红色 。
(4)甲、乙、丙同学分析了实验现象,为确定溶液的酸碱性,又进行下列实验:
甲同学用 来测定溶液,原因是 。
乙同学向溶液中滴加 ,使溶液中红色刚好褪去。因为造成(3)中溶液的红色仍不消失的原因是 。
【解释与结论】
用硫酸钠增强水的导电性时,电解后溶液混合均匀,呈中性。
【交流与反思】
甲同学取55 g质量分数为2%的硫酸钠溶液进行电解,消耗了5 g水,则电解后硫酸钠溶液的质量分数为 。
甲同学的老师上课时用NaOH增强水的导电性,电解后溶液的碱性 。
乙同学的老师上课时用H2SO4增强水的导电性,电解后溶液的酸性 。
答案
【实验与探讨】(1)碱 酸
(2)不足(或酸液残留在管壁上等)
(3)恰好褪去(或立即消失)
(4)pH试纸
实验中滴加酚酞的溶液变为无色,可能呈中性,也可能因酸过量而显酸性,故用pH试纸来确认。
稀硫酸(或酸)
乙同学用pH试纸测定管②电极附近溶液时消耗了少量酸
【交流与反思】2.2% 增强 增强
知识点:综合应用题
略
略










