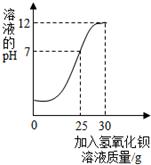
为测定某未知浓度的Ba(OH)2溶液的溶质质量分数,取某稀硫酸溶液20 g,逐滴加入Ba(OH)2溶液30 g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示),过滤后得滤液47.67 g,则Ba(OH)2溶液的溶质质量分数为( )
(可能用到的相对原子质量:H-1,O-16,S-32,Ba-137)
- A.6.84%
- B.13.68%
- C.20.52%
- D.27.36%
答案
正确答案:A
知识点:化学方程式的计算
根据图象可知,当加入25 gBa(OH)2溶液时,与稀硫酸恰好完全中和,此后所加Ba(OH)2
溶液不再发生反应,根据质量守恒定律可计算加入25g Ba(OH)2溶液恰好完全反应时生成
沉淀BaSO4的质量;利用沉淀BaSO4的质量,根据化学方程式,计算出25g Ba(OH)2溶液中
溶质Ba(OH)2的质量,从而可求出Ba(OH)2溶液的溶质质量分数。
根据质量守恒定律,生成的BaSO4质量为:20g+30 g-47.67g=2.33 g;
设参加反应的Ba(OH)2的质量为x,则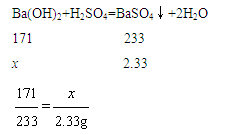
解得x=1.71g
此时恰好完全反应,消耗Ba(OH)2的质量为25g,
故Ba(OH)2的溶质质量分数=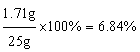 。
。
故选A。
略








